ÉDITION SPÉCIALE MYÉLOME
60TH ASH ANNUAL MEETING
1 au 4 décembre 2018, San Diego, États-Unis
Enfin les premiers Bites dans le myélome !
D’après la communication orale de Topp M.S et al. Treatment with AMG 420, an Anti-B-Cell Maturation Antigen (BCMA) Bispecific T-Cell Engager (BiTE®) Antibody Construct, Induces Minimal Residual Disease (MRD) Negative Complete Responses in Relapsed and/or Refractory (R/R) Multiple Myeloma (MM) Patients: Results of a First-in-Human (FIH) Phase I Dose Escalation Study.
Abstract 1009 – 60th American Society of Hematology (ASH) Annual Meeting, San Diego, Décembre 2018.
Evènement à San Diego, le premier essai Bites dans le myélome a été présenté : AMG 420 : anti BCMA et anti CD3 permettant une lyse cellulaire médiée par les lymphocytes T via la voie Fas. Ce premier essai chez l’homme est une étude de phase 1 avec escalade de dose pour 10 cycles selon la réponse. Les objectifs primaires étaient la tolérance et la sécurité afin de déterminer la dose maximale tolérée et l’évaluation de l’effet anti-tumorale. Les patients avec un myélome en rechute ou en progression après deux lignes de traitements antérieures comprenant un inhibiteur du protéasome et un immunomodulateur étaient incluables. Les formes extramédullaires, les leucémies à plasmocytes, l’atteinte du système nerveux central étaient exclus. Au total 27 patients ont été inclus dont 13 % de haut risque cytogénétique, avec une médiane de traitements antérieurs de 4 (26 % daratumumab ; 83 % autogreffés). La dose maximum tolérée dans cette étude était de 400 μg par jour (2 DLT à la dose de 800 μg /j : CRS de grade 3 et une neuropathie périphérique de grade 3).
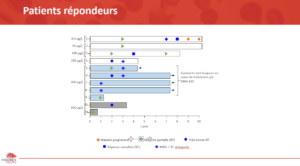
Aucune toxicité neurologique centrale de grade 3 ou 4 n’a été constatée. Deux décès ont été rapportés suite à des infections : l’un à adénovirus et l’autres aspergillus dont le lien avec AMG 420 n’a pas été fait. Les deux cas de neuropathies périphériques ont été améliorés après perfusion d’immunoglobulines polyvalentes et corticoïdes avec un retour à l’état clinique antérieur. Un effet anti-tumoral a pu être observé pour 7 patients sur 10 à la dose de 400 mg dont 4 MRD négatives et 3 réponses complètes à plus faibles doses (Figure 1).
Ces premiers résultats encourageants ont permis une extension de l’étude avec une phase 1b qui commencera début 2019.
Alexis Talbot